目次
- はじめに(本記事の読み方)
- 学習の方針と『3ステップ解法』
- 頻出良問10選(問題+図+詳しい解説)
- 問1〜3:水溶液の性質(溶解度・濃度・中和)
- 問4〜6:気体の性質と発生(捕集法・密度比較・実験)
- 問7〜8:物質の変化(燃焼・質量保存・酸化還元)
- 問9〜10:金属の性質(反応性・イオン化傾向)
- よくある計算ミスとチェックリスト
- 家庭でできる実験と練習問題(演習)
- まとめ:入試で化学を得点源にするために
1. はじめに(本記事の読み方)
中学入試の化学では、暗記だけでは通用しません。重要なのは「実験の意味をイメージ化」し、出題パターンごとに『解き方の型』を身につけることです。本記事は**“問題→図でイメージ→解答手順→よくある間違い”**という順でまとめています。
2. 学習の方針と『3ステップ解法(化学版)』
目的:出題意図を素早く掴み、確実に完成した答案を書く。
3ステップ解法
ステップA(性質把握):登場する物質の性質を即座に確認する(酸/塩基、水溶性、気体の特徴、重さの比較など)。
ステップB(実験と図の再現):問題文で与えられた器具・操作を図で再現し、実験で何が起きるかを線で示す(生成物の移動、気体の上昇・沈降、溶解→析出の流れなど)。
ステップC(計算と単位チェック):定義(質量パーセント濃度、溶解度、モルではなく比で解ける問題)に基づき、単位と比を最優先で計算。最後は単位と答えの大きさが妥当かチェックする。
解答時の心がけ:図を必ず一つは描く。入試の配点は図や理由を問う問題で差がつきます。
3. 頻出良問10選(問題+図+詳解)
以下は中学入試でよく出る典型問題を、問題→図解→解法→解答例→注意点の順でまとめたものです。
問1(溶解度曲線)
問題(例):ある物質Aの溶解度は下の表の通りです。50℃の飽和水溶液200 gを冷却して10℃まで下げると、何 g の結晶が取り出せるか。
図(解説用):溶解度曲線を横軸に温度、縦軸に溶解度(g/100 g水)を描き、50℃と10℃の位置を点で示す。飽和水溶液200 g の『溶媒(=水)重さ』を求めるための補助線を引く。
解法:
- 50℃での溶解度(例:40 g/100 g水)→飽和水溶液中の溶質量を求める。
- 溶液の合計200 g から水の質量を求め(溶質+水=200 g)、10℃での溶解度(例:20 g/100 g水)により再度飽和状態の溶質量を求める。
- 初めの溶質量 − 再飽和溶質量 = 結晶として取り出せる量。
ポイント:『溶解度は g/100 g 水』であることを忘れない。溶液の“全体質量”で与えられたときは、まず水の質量を求める一手間が必要。
よくあるミス:溶解度の単位を勘違いして、100 g ではなく溶液全体を基準に計算する。
問2(質量パーセント濃度の混合)
問題(例):濃度10%の食塩水100 gと濃度20%の食塩水50 gを混ぜたときの濃度は何 % か。
図(解説用):
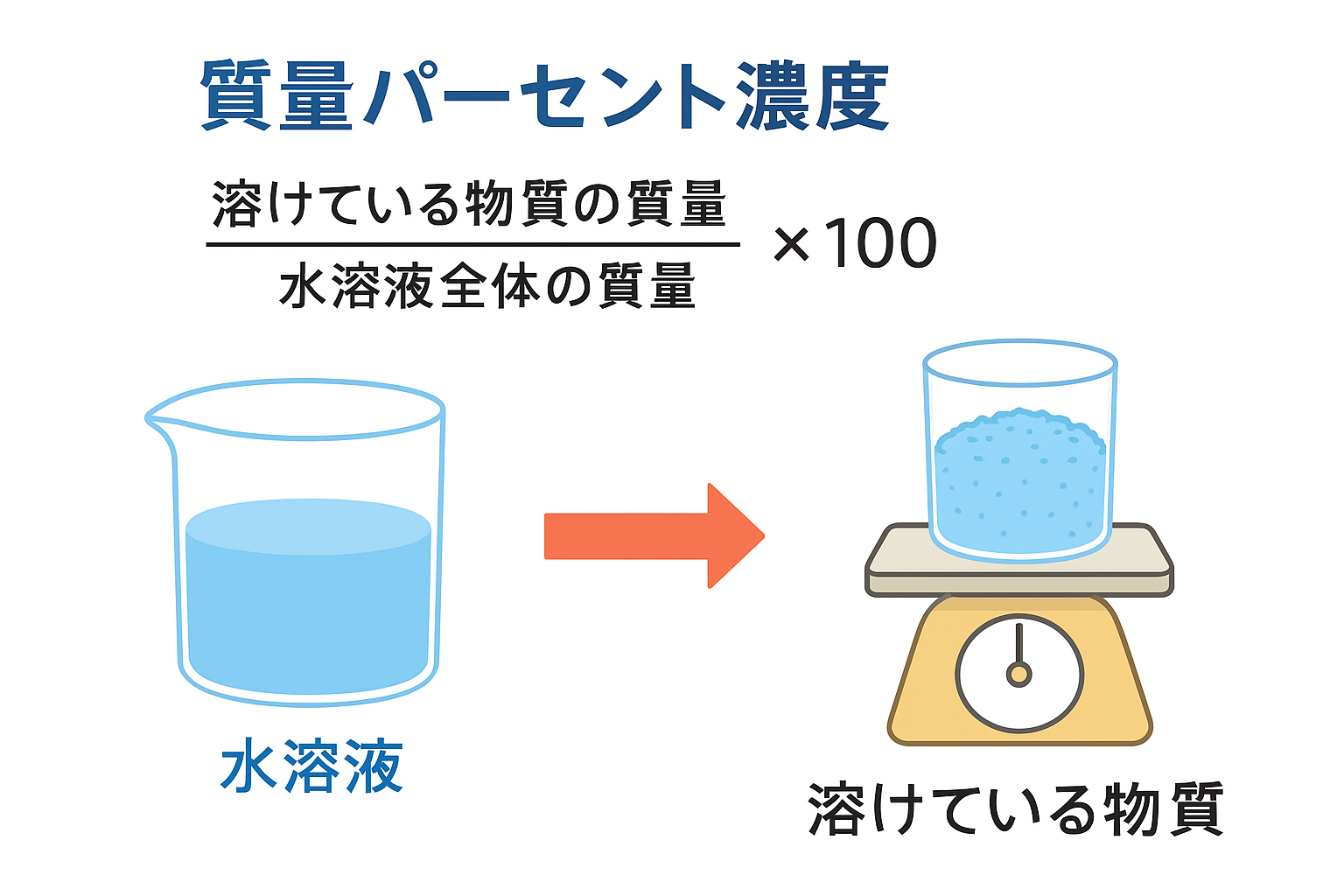
解法:
- 各溶液の溶質量を計算(10% の100 g → 10 g、20% の50 g → 10 g)。
- 溶質合計=20 g、溶液全体=150 g → 濃度=20/150=13.3%。
チェックリスト:必ず溶質の質量と溶液全体の質量を分けて考える。
問3(中和と体積・濃度の関係)
問題(例):0.1 mol/L の塩酸20 mL を中和するのに必要な水酸化ナトリウム(1 mol/L)は何 mL か(反応は HCl + NaOH → NaCl + H2O)。
図(解説用):反応式を書き、プロトン(H+)と OH- の等価関係を矢印で図示。モル(mol/L × L)で計算する補助線を示す。
解法:mol を使って計算:HCl の mol = 0.1 mol/L × 0.020 L = 0.002 mol。NaOH は 1:1 反応なので同じ mol が必要 → 必要体積 = 0.002 mol ÷ 1.0 mol/L = 0.002 L = 2.0 mL。
ポイント:単位(L と mL)を混ぜない。途中で mL ⇄ L の変換を明確に書く。
問4(気体の捕集法の選択)
問題(例):ある気体Bは水にほとんど溶けず、空気より軽い。この気体を捕集する方法はどれか(選択肢:水上置換、上方置換、下方置換)。
図(解説用):3 種類の捕集法の簡単図を並べ、それぞれの原理(『水を使う』『空気の上に気体が上がる』『空気の下に沈む』)を矢印で示す。
解法:空気より軽く、水に溶けにくい → 上方置換。
覚え方:『水に溶ける→水上置換。軽い→上方、重い→下方』と単純化して覚える。
問5(代表的な気体発生実験)
問題(例):二酸化炭素はどの反応で発生し、どの捕集法が使われるか。
図(解説用):石灰石(炭酸カルシウム)+塩酸の装置図を描き、発生した気体を水上置換で捕集する様子を示す(CO2 は水に少し溶けるが、一般的には水上置換で扱う)。
ポイント:実験で使う薬品と器具をセットで覚える(例:酸+炭酸塩→CO2、酸化剤+過酸化水素→O2 など)。
問6(気体の密度比較)
問題(例):同じ条件下で、H2、O2、CO2 の密度を比べ、空気より軽いか重いかを答えよ。
図(解説用):分子量を並べた表(H2:2、O2:32、CO2:44)と、空気の平均分子量(約29)を示し、比較する矢印を描く。
解法:分子量で比較→ H2(2)<空気(29)→軽い、O2(32)>空気→ほぼ同じかやや重い、CO2(44)>空気→重い。
注意:空気の分子量は約29であることを覚えておくと便利(入試では数値は与えられることが多い)。
問7(質量保存の法則)
問題(例):密閉容器内で炭素 (C) と酸素 (O2) が反応して CO2 になる実験で、容器の質量はどうなるか。
図(解説用):密閉容器の断面図に反応前後の粒子(C と O の原子)を描き、原子数が変わらないことを図示する。
解法:密閉容器で物質の出入りがなければ、質量は保存される → 質量は変わらない。
深掘り:見かけ上の増減は気体の発生や析出を伴う場合に起きるが、密閉系なら原子レベルで保存を説明できる。
問8(酸化と還元の基礎)
問題(例):銅を加熱すると性質や質量はどう変化するか(酸化の例)。
図(解説用):銅(Cu)と酸素(O2)が結び付いて酸化銅(CuO)になる模式図。酸素が結びつくときに質量が増える様子を示す。
解法:酸化により酸素が取り込まれるため、質量は増える(開放系で酸素が外から入るため)。反対に還元は酸素を失う過程で質量が減る場合がある。
注意点:単に『物が黒くなる=質量が増える』ではない。必ず反応の相手(酸素など)がどこから来るかを考える。
問9(金属の反応性)
問題(例):マグネシウムと鉄をそれぞれ塩酸に入れたときの反応の速さや生成物の違いについて説明せよ。
図(解説用):金属の活性順(イオン化傾向)を簡単な棒グラフで示し、酸と反応して水素が発生する様子を図示。
解法(要点):イオン化傾向が大きい金属(マグネシウムなど)は酸と激しく反応して水素を発生する。鉄は反応するが速度は遅い。
学習ポイント:代表的な金属の反応(Na、Mg、Fe、Cu)を反応性の強い順に覚えると良い。入試では具体的な数字より傾向が問われる。
問10(金属元素の分類と性質)
問題(例):金属と非金属の性質を挙げ、具体的な実験でどのように区別するか。
図(解説用):導電性、光沢、延性・展性、熱伝導性などのチェックリストと、簡単な実験(導電性テスター、火で加熱しての反応)をフローチャート形式で示す。
解法(要点):金属は電気を通し、熱伝導が良く、光沢がある。水や酸との反応での違い(Na は激しく反応、Cu は反応しにくい)を示して区別する。
4. よくある計算ミスとチェックリスト
共通ミスと対策
- 単位の混在(mL と L の混同)→ 解答欄に単位を書いてから計算。
- 『溶解度(g/100 g 水)』と『質量パーセント(%)』の混同→定義を問題の冒頭に書く。
- 桁の桁落ち(0.2 を 2 と見間違う等)→途中で必ず一度電卓以外で近似値を紙に書く。
- 図を描かない→図を描く癖をつける。図で 80% は解ける。
チェックリスト(解答前)
- 物質の性質(酸/塩基/気体の性質)を書いたか?
- 単位(g, mL, L, %)を揃えたか?
- 計算途中で比や割合を確認したか?
- 結果が理屈と合っているか(例:気体が空気より軽いのに下方置換で回収していないか)?
5. 家庭でできる実験と練習問題
安全に注意しながらできる観察例
- 食塩水の作成と蒸発で濃度の変化を観察
- 石灰水で二酸化炭素の発生を確認(息を吹きかけて白濁)
- 銅線を加熱して(教材用の小スケール)変化を観察(必ず換気・保護具)
演習問題(入試レベル)
- ある溶液は質量パーセント 15% の硫酸銅水溶液である。溶液 120 g 中の溶質は何 g か。
- 0.2 mol/L の硝酸 50 mL を中和するのに必要な水酸化ナトリウム(1.0 mol/L)は何 mL か。
- ある気体が水にあまり溶けず、空気より重い時の捕集法を答え、理由を簡潔に述べよ。
解答、解説は後日このサイト上にUPします。
6. まとめ:入試で化学を得点源にするために
- **図で『見える化』**する癖をつける(溶液・気体・反応の流れ)。
- 定義を最優先で使う(濃度、溶解度、mol の基礎)。
- 3ステップ解法(性質把握→図→計算)を全問題で実践する。
- 間違えた問題は、必ず『図を描いて説明できる』まで復習する。
最後に――化学は『小さな法則の組合せ』でできています。良問を何度も繰り返し、“パターン”を体に染み込ませれば、本番での安定した得点につながります。必要なら、この文書を元に「問題集用のプリント」を作成して差し上げます。ご希望があれば、良問の具体的な出題文と図(試験形式)を10問セットで作ります。
